首页 条形码新闻知识 条形码知识
如何遵守和从哪里开始UDI标签规定解释
UDI标签规定解释:如何遵守和从哪里开始
作者: JENNA WAGNER / 日期: 24/10/2024 / 主题: 器材, 健康保健, 标签设计, 法规遵从性, 标签设计
在当今的医疗保健领域,确保患者的安全和维护高效的供应链对于医疗设备制造商至关重要。唯一设备标识符 (UDI) 系统是实现这一目标的关键组成部分。但 UDI 标签到底是什么,为什么它很重要,以及制造商如何遵守其法规? 本博客将指导您了解 UDI 标签法规,分解合规性的基本要素。要更深入地了解医疗设备、药品和医疗保健标签要求和最佳实践的具体内容,请查看我们的电子书:生命科学标签与合规。 什么是 UDI 标签?由美国食品药品监督管理局 (FDA) 制定的 UDI 系统最终规则要求医疗器械贴标商(通常是制造商)在设备标签和包装上包含 UDI,并将设备信息提交到全球唯一设备标识数据库 (GUDID)。 这有助于充分识别在美国销售的医疗器械,从制造到分销再到患者使用。医疗设备的范围从医用手套和压舌板到心脏起搏器和机器人手术系统。 为什么 UDI 很重要UDI 标签不仅关乎法规遵从性,还关乎安全性和效率。
UDI 是全球推动协调医疗器械法规的一部分,其标准被 FDA 和欧洲医疗器械法规 (EU MDR) 采用。
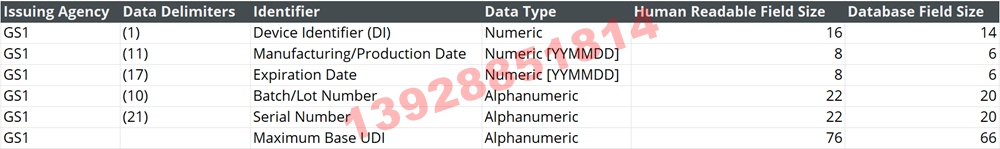
UDI 由什么组成UDI 包含两个部分: 1. 设备标识符 (DI):DI 是 UDI 的固定部分,用于标识贴标机和设备的特定版本或型号。它不会改变,并充当设备识别系统的支柱。来自 GS1(FDA 认可的发行机构)的全球贸易项目代码® (GTIN)® 可用作 DI。 2. 生产标识符 (PI):PI 是一个可变部分,可能包括以下一项或多项:
这些信息有助于跟踪设备的生产和使用寿命,从而在必要时更轻松地管理和调用设备。
GS1 易于阅读的纯文本 UDI 示例: (01)51022222233336(11)141231(17)150707(10)A213B1(21)1234
如何遵守 UDI 标签要求?为了遵守 UDI 标签法规,制造商必须满足 UDI 在其设备和包装上的显示方式的特定要求。以下是关键要求:
人类可读和机器可读格式所有 UDI 必须以人类可读(纯文本)和机器可读格式显示在标签和包裹上。机器可读部分通常使用自动识别和数据捕获 (AIDC) 技术进行编码,例如条形码或射频识别 (RFID)。
标准化的日期格式设备标签上的任何日期(如有效期或生产日期)都必须遵循标准化格式:**YYYY-MM-DD**。这确保了全球医疗器械市场的一致性和清晰度。
在 CODESOFT条形码标签软件中创建的符合 UDI 的标签示例。
我从哪里开始使用 UDI 标签?遵守 UDI 法规似乎令人生畏,但通过遵循明确的流程,制造商可以确保他们符合 FDA 的要求。
第 1 步:从 FDA 认可的发证机构获取 UDI创建 UDI 标签的第一步是联系 FDA 认可的发行机构。FDA 已批准三个发行机构运行分配 UDI 的系统:
贴标机必须直接联系其中一个发卡机构,以使用他们的系统为其设备发卡 UDI。
步骤 2:向 GUDID 提交设备信息获得 UDI 后,制造商必须向 GUDID 提交设备信息。该数据库可公开访问,可作为医疗保健专业人员、监管机构和患者识别医疗设备的参考。 GUDID 仅包含 UDI 的 DI 部分,该部分用于在数据库中查找有关设备的信息。虽然 GUDID 不存储 PI,但它具有标志来显示哪些 PI 详细信息是 UDI 的一部分。 有关访问 GUDID 的更多信息,您可以访问 FDA 的网站。
第 3 步:评估您当前的标签流程标签软件确保您的标签软件可以同时支持人类可读和机器可读格式。它还应处理各种条形码类型,例如 GS1-128 或 GS1 DataMatrix,并提供为 PI 生成唯一序列号或批号的灵活性。 如果您的标签软件不支持这些特性和功能,那么是时候升级了。CODESOFT RFID 和条形码标签设计软件等解决方案提供基于设备的唯一标识符(DI、PI)的动态标签创建,并与 Excel 和 Access 等数据库或企业资源规划 (ERP) 系统和产品生命周期管理 (PLM) 系统等业务系统轻松集成。 下载 CODESOFT 的 30 天免费试用版,并使用以下有用的视频说明:
在试用期间,您还可以拨打13928851814 联系 专业 客户支持(如果您有任何疑问)。
标签打印机
您的打印机还必须能够制作带有可读条形码的高质量标签,以满足 UDI 标准。选择与您的标签软件兼容并提供可靠性能的打印机品牌。 TEKLYNX 为 Zebra、TSC、SATO、Epson 和 Honeywell 等品牌开发了 4,000 多个本机标签打印机驱动程序,为您的条形码标签需求提供最佳的整体质量。阅读我们的白皮书,了解使用 TEKLYNX 打印机驱动程序的好处。 现在,您已经了解了 UDI 标签,因此这是一个快速的合规性清单:
通过执行这些步骤,您可以确保您的医疗器械满足所有 UDI 标签要求,从而确保您的商品合规和患者安全。
超越合规性:UDI 标签的真正影响UDI 标签不仅仅是为了遵守 FDA 法规,**还是为了让医疗保健更安全、更高效。**从提高产品可追溯性到简化召回,UDI 标签的好处远远超出了法规遵从性。 如果您正在寻找标签软件提供商来帮助实现 UDI 合规性,请考虑使用我们的方案。我们的解决方案提供与您现有系统的无缝集成,支持所有 UDI 标签格式,并提供可靠的客户支持。正如 QTS 的 Todd Engelken 所说:“我们对遵守 UDI 标准非常有信心。我可以肯定地说,我们与 TEKLYNX 的选择是正确的。 有了正确的工具、知识和支持,遵守 UDI 标签法规就不一定很困难。TEKYNX 随时为您提供帮助。 或者下载 CODESOFT 的 30 天免费试用版,其中包括 UDI 标签示例。 |